本網(wǎng)訊 近日,中南大學(xué)生命科學(xué)學(xué)院劉靜教授團(tuán)隊在紅細(xì)胞生成(erythropoiesis)精細(xì)調(diào)控機(jī)制研究方面取得系列重要進(jìn)展,相關(guān)成果相繼發(fā)表于《核酸研究》(Nucleic Acids Research)和《基因組學(xué)、蛋白質(zhì)組學(xué)與生物信息學(xué)》(Genomics, Proteomics & Bioinformatics)。該研究從轉(zhuǎn)錄調(diào)控與染色質(zhì)重塑、以及轉(zhuǎn)錄后加工與選擇性多聚腺苷酸化(APA)兩個層面,系統(tǒng)揭示了紅系發(fā)育過程中的關(guān)鍵分子調(diào)控網(wǎng)絡(luò),為紅系相關(guān)疾病的機(jī)制解析及潛在干預(yù)策略的開發(fā)提供了重要的理論依據(jù)。
紅細(xì)胞生成是維持機(jī)體氧運輸與血紅蛋白穩(wěn)態(tài)的關(guān)鍵生理過程,每秒需生成約兩百萬個紅細(xì)胞以滿足機(jī)體需求。紅系發(fā)育異常與貧血、骨髓增生異常綜合征等疾病密切相關(guān),深入解析其調(diào)控機(jī)制具有重要科學(xué)意義和潛在臨床價值。轉(zhuǎn)錄因子GATA1(位于X染色體上的關(guān)鍵轉(zhuǎn)錄因子基因名)被公認(rèn)為紅系分化的核心調(diào)控因子,但其轉(zhuǎn)錄上游調(diào)控網(wǎng)絡(luò)尚未完全闡明;同時,紅系祖細(xì)胞BFU-E、CFU-E(紅系造血祖細(xì)胞的兩個關(guān)鍵亞群)的增殖與分化受多層級轉(zhuǎn)錄后調(diào)控,其關(guān)鍵機(jī)制仍有待深入解析。
在發(fā)表于《核酸研究》的研究中,研究團(tuán)隊發(fā)現(xiàn)染色質(zhì)重塑因子HLTF(一種解旋酶樣轉(zhuǎn)錄因子)可直接結(jié)合GATA1啟動并促進(jìn)其轉(zhuǎn)錄表達(dá)。體內(nèi)外模型證實,HLTF缺失導(dǎo)致GATA1顯著下調(diào),進(jìn)而抑制細(xì)胞增殖、誘導(dǎo)凋亡并阻滯紅系分化。多組學(xué)聯(lián)合分析顯示,HLTF缺失引起紅系基因啟動子區(qū)域染色質(zhì)可及性降低,并削弱GATA1全基因組結(jié)合能力。值得注意的是,HLTF不僅作為GATA1的上游調(diào)控因子,還可與GATA1相互作用,招募TAL1(干細(xì)胞白血病基因)、BRG1(染色質(zhì)重塑復(fù)合體的核心亞基)等協(xié)同調(diào)控;同時GATA1反向激活HLTF表達(dá),二者形成正反饋調(diào)節(jié)環(huán)路,共同維持紅系分化相關(guān)轉(zhuǎn)錄程序的穩(wěn)定性。臨床數(shù)據(jù)分析進(jìn)一步揭示,HLTF在真性紅細(xì)胞增多癥(PV)等疾病中顯著失調(diào),提示其或為紅系疾病的潛在分子標(biāo)志物與治療靶點。
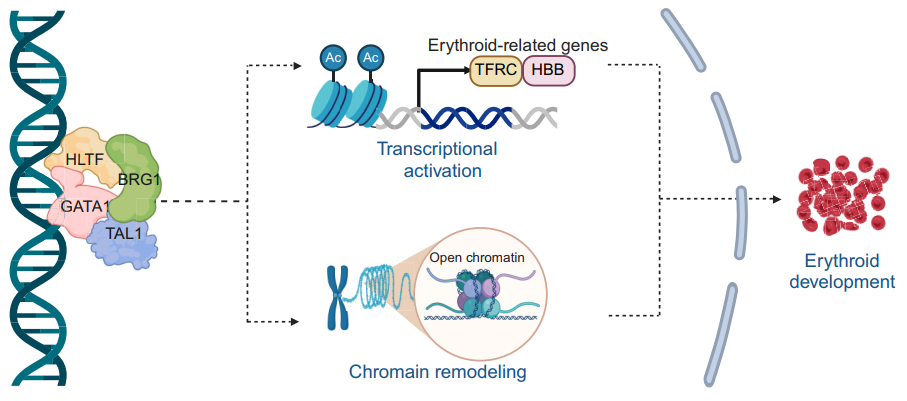
HLTF與GATA1協(xié)同激活紅細(xì)胞發(fā)育過程中的轉(zhuǎn)錄程序與染色質(zhì)重塑
另一項發(fā)表于《基因組學(xué)、蛋白質(zhì)組學(xué)與生物信息學(xué)》的研究聚焦紅系分化中的選擇性多聚腺苷酸化(APA)。團(tuán)隊通過整合不同階段轉(zhuǎn)錄組數(shù)據(jù),系統(tǒng)構(gòu)建了動態(tài)APA圖譜,發(fā)現(xiàn)紅系分化早期普遍發(fā)生3′UTR(真核生物mRNA分子中位于終止密碼下游尾巴之前的非編碼區(qū)域)縮短,且與細(xì)胞周期和RNA調(diào)控通路密切相關(guān)。PABPC1(多聚腺苷酸結(jié)合蛋白胞質(zhì)1號)被鑒定為介導(dǎo)BFU-E向CFU-E轉(zhuǎn)變過程中APA的關(guān)鍵因子。功能實驗證實,PABPC1敲低可抑制紅系祖細(xì)胞增殖、促進(jìn)細(xì)胞凋亡并阻礙CFU-E集落形成。結(jié)合三代全長轉(zhuǎn)錄組測序,研究揭示PABPC1通過APA調(diào)控TSC22D1(一個編碼亮氨酸拉鏈轉(zhuǎn)錄因子的基因)表達(dá),影響紅系祖細(xì)胞擴(kuò)增與分化,為紅細(xì)胞生成的轉(zhuǎn)錄后調(diào)控機(jī)制提供了新見解。
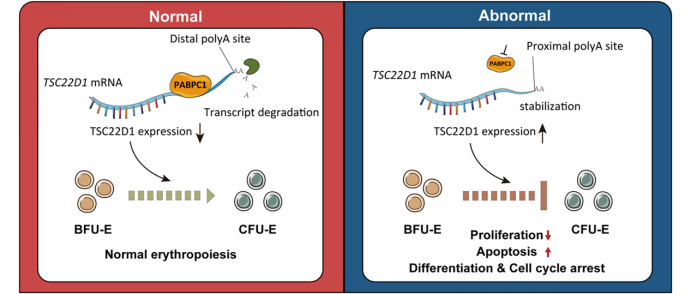
PABPC1通過調(diào)控可變多聚腺苷酸化事件影響紅系祖細(xì)胞增殖
兩項研究分別從“轉(zhuǎn)錄—染色質(zhì)”調(diào)控與“轉(zhuǎn)錄后加工”兩個關(guān)鍵層面深化了對紅細(xì)胞生成多層級調(diào)控網(wǎng)絡(luò)的理解,為紅系相關(guān)疾病的發(fā)生機(jī)制研究及精準(zhǔn)干預(yù)策略的探索提供了重要的理論依據(jù)。
(一審:范泓洋 二審:唐瀟珺 三審:韓艷)




















